Informacje o produkcie
|
Nazwa produktu |
Kot. NIE. |
Spec. |
|
Zestaw do wykrywania apoptozy komórek tunelowych Click-iT 647 |
G1509-50T |
50T |
Opis produktu/wprowadzenie
Łamanie chromosomalnego DNA podczas apoptozy jest procesem stopniowym i etapowym. Chromosomalny DNA jest najpierw rozkładany na duże segmenty ({0}} kb przez endogenne hydrolazy kwasu nukleinowego, a następnie około 30% chromosomalnego DNA jest losowo wycinane pomiędzy jednostkami nukleosomu w obecności Ca2+ i Mg{{3} } zależne endonukleazy kwasu nukleinowego, tworząc multimery nukleosomalnego DNA o 180-200 bp. Zatem w późnej apoptozie DNA ulega degradacji na fragmenty o 180-200 bp, a na uszkodzonym genomowym DNA zostaje odsłonięta duża liczba końców 3'-OH. Terminalna transferaza deoksynukleotydowa (TdT) jest niezależną od matrycy polimerazą DNA, która katalizuje wbudowywanie deoksyrybonukleotydów do końców 3'-OH uszkodzonych cząsteczek DNA. Dlatego zestaw do wykrywania apoptozy komórek TUNEL (TdT mediated dUTP Nick End Labeling) może być stosowany do wykrywania uszkodzeń jądrowego DNA w komórkach tkankowych podczas późnej apoptozy.
Zasada jest taka, że pod działaniem enzymu TdT EdUTP (dUTP z modyfikacją alkinową) jest domieszkowany na końcu 3'-OH odsłoniętym podczas rozerwania genomowego DNA, a grupa alkinowa reaguje z barwnikiem azydkowym w katalizowanej reakcji tworzenia pierścienia przez jednowartościowy jon miedzi (reakcja kliknięcia), wprowadzając w ten sposób ugrupowanie fluorescencyjne w ukierunkowany sposób. W tym zestawie zastosowano azydek iF647, dzięki czemu można go wykryć za pomocą mikroskopu fluorescencyjnego lub cytometrii przepływowej (wzbudzenie iF647 656 nm, emisja 670 nm). W porównaniu do innych zmodyfikowanych dUTP, EdUTP ma mniejszą oporność miejsca przestrzennego i łatwiej jest domieszkować końce DNA przez TdTase.
Zestaw ten ma szeroki zakres zastosowań i jest odpowiedni do wykrywania apoptozy w skrawkach tkanki parafinowej, skrawkach zamrożonych tkanek, komórkach pełzających i rozmazach komórkowych.

oznaczanie reakcji od kliknięcia do reakcji
Rysunek 1. Schemat ideowy działania zestawu TUNEL opartego na technologii kliknięcia
Warunki przechowywania i wysyłki
Statek z mokrym lodem; Przechowywać w temperaturze -20 przez 12 miesięcy.
Zawartość produktu
|
Numer komponentu |
Część |
G1509-50T |
|
G1509-1 |
Rekombinowany enzym Tdt |
50 μL |
|
G1509-2 |
Mieszanka etykiet EdUTP |
250 μL |
|
G1509-3 |
Bufor równoważący |
5×1ml |
|
G1509-4 |
Proteinaza K (200 ug/ml) |
1 ml |
|
G1509-5 |
Barwnik azydkowy iF647 |
80 μL |
|
G1509-6 |
Bufor reakcyjny A |
5×1ml |
|
G1509-7 |
Bufor reakcyjny B |
60 μL |
|
G1509-8 |
Dodatek reakcyjny (Odczynnik C) |
2×100 mg |
|
Podręcznik |
1 szt |
|
Wstępne eksperymenty
1. Bufor fosforanowy PBS (zalecany G0002 lub G4202);
2. Roztwór stały: 4% paraformaldehyd rozpuszczony w PBS, pH 7,4 (zalecany G1101);
3. Roztwór rozbijający membranę: 0,1% Triton X-100 rozpuszczony w 0,1% cytrynianie sodu (zalecany G1204);
4. 0,2% Triton X-100 przygotowany w PBS; 0.1% Triton X-100 przygotowany w PBS zawierającym 5 mg/ml BSA;
5. Do barwienia jądra komórkowego należy podać własny DAPI (2 µg/mL), Hoechst 33258 lub PI (1 µg/mL) (zalecane G1012, G1011, G1021);
6. DNaza I (G3342) do eksperymentów z kontrolą pozytywną;
7. Dodatek reakcyjny (Odczynnik C) odwirowuje się przy niskiej prędkości, 100 mg proszku rozpuszcza się w 1 ml ultraczystej wody (gotowej do użycia), dozuje się 100 µl i przechowuje w temperaturze -20, pozostawiając pozostały proszek do użytku zapasowego; (Odczynnik C łatwo się utlenia, należy unikać długotrwałego kontaktu z powietrzem. Po sporządzeniu roztworu wodnego zdecydowanie zaleca się podzielenie go na małe porcje do użycia; Po przetestowaniu wodnego roztworu Odczynnika C, kolor niewielka zmiana, kliknięcie systemu reakcji może nadal przebiegać normalnie, a jeśli pokaże kolor brązowy, oznacza to, że komponent został unieważniony)
8. Jeżeli kolor tła wyniku jest zbyt ciemny, może to być spowodowane niewystarczającym przemyciem i pozostałościami utrwalacza podczas doświadczenia;
9. Uważaj, aby dodać ciecz reakcyjną po kolei i dobrze wymieszaj podczas dodawania;
10. Dla własnego zdrowia i bezpieczeństwa podczas pracy należy nosić fartuch laboratoryjny i rękawiczki.
Protokół/procedury testu
1. Przygotowanie próbki
A. Skrawki tkanek zatopione w parafinie
A. Skrawki tkanki parafinowej zanurzono w ekologicznym, klarownym roztworze do usuwania wosku (G1128) na 5-10 min w temperaturze pokojowej i powtórzono 3 razy; Następnie namoczyć w bezwodnym etanolu na 5 minut i powtórzyć dwukrotnie; Na koniec namoczyć w gradientowym etanolu (85%, 75% i woda podwójnie destylowana) raz na 5 minut;
B. Delikatnie zwilż skrawek PBS i usuń nadmiar płynu wokół próbki, użyj pióra PAP, aby narysować małe kółko w odległości 2-3 mm od tkanki wzdłuż obwodowego konturu tkanki, aby ułatwić dalsze przetwarzanie przepuszczalności i operacje znakowania równowagi, wykonaj nie dopuścić do wyschnięcia próbki podczas eksperymentów i przechowywać przetworzone próbki w wilgotnym pudełku, aby próbki były wilgotne;
C. Przygotowanie roztworu roboczego Proteinazy K: Rozcieńczyć roztwór podstawowy Proteinazy K (200 µg/ml) PBS jako rozcieńczalnikiem w stosunku 1:9, aby uzyskać końcowe stężenie 20 µg/ml;
D. Dodać 100 µl powyższego roztworu roboczego Proteinazy K do każdej próbki, aby była całkowicie pokryta i inkubować w temperaturze 37 stopni przez 20 minut;
Uwaga: Traktowanie proteinazą K przyczynia się głównie do przenikania odczynników barwiących w kolejnych etapach tkanek i komórek, a czas jej inkubacji jest zbyt długi lub zbyt krótki, aby wpłynąć na skuteczność późniejszego znakowania, w celu uzyskania lepszych wyników, inkubacja czas można zoptymalizować w zależności od rzeczywistej sytuacji.
mi. Przemyć próbki poprzez zwilżenie roztworem PBS 3 razy po 5 minut za każdym razem (Proteinazę K należy umyć do czysta, w przeciwnym razie będzie to zakłócać późniejszą reakcję znakowania). Obrobione próbki umieszczono w wilgotnym pudełku, aby próbki były wilgotne;
F. (Krok opcjonalny) Usuń nadmiar płynu z próbki, dodaj odpowiednią ilość kropelek roztworu rozrywającego membranę do tkanki, całkowicie infiltruj tkankę i poddawaj działaniu przez 20 minut w temperaturze pokojowej; po zakończeniu procesu rozbijania membrany próbkę podobnie przemywa się roztworem PBS 3 razy, za każdym razem po 5 min; traktowaną próbkę umieszcza się w wilgotnym pudełku, aby utrzymać wilgotność próbki.
B. Sekcja zamrożona tkanki
A. Zamrożone skrawki tkanki zanurza się w utrwalaczu, inkubuje i utrwala przez 10-15 min w temperaturze pokojowej;
B. Skrawki tkanki usuwa się z utrwalacza i umieszcza pod wyciągiem w celu naturalnego wyschnięcia;
C. Skrawki tkanek zwilża się i przemywa oczyszczoną wodą lub PBS w celu usunięcia pozostałości utrwalacza z próbki;
D. Za pomocą pisaka histochemicznego narysować małe kółko w odległości 2-3 mm od tkanki wzdłuż jej obwodowego konturu, aby ułatwić dalsze przetwarzanie przepuszczalności i znakowanie równowagi, nie dopuścić do wyschnięcia próbki podczas eksperymentów i zachować przetworzone próbki w wilgotnym pudełku, aby próbki były wilgotne;
mi. Przygotowanie roztworu roboczego Proteinazy K: Rozcieńczyć roztwór podstawowy Proteinazy K (200 µg/ml) PBS jako rozcieńczalnikiem w stosunku 1:9, aby uzyskać końcowe stężenie 20 µg/ml;
F. Dodać 100 µl powyższego roztworu roboczego Proteinazy K do każdej próbki, aby była całkowicie pokryta i inkubować przez 10 minut w temperaturze pokojowej;
Uwaga: Traktowanie proteinazą K przyczynia się głównie do przenikania odczynników barwiących w kolejnych etapach tkanek i komórek, a czas jej inkubacji jest zbyt długi lub zbyt krótki, aby wpłynąć na skuteczność późniejszego znakowania, w celu uzyskania lepszych wyników, inkubacja czas można zoptymalizować w zależności od rzeczywistej sytuacji.
G. Przemyj próbkę 2-3 razy roztworem PBS, aby usunąć nadmiar płynu (Proteinazę K należy umyć do czysta, w przeciwnym razie będzie to zakłócać późniejszą reakcję znakowania) i trzymaj traktowaną próbkę w wilgotnym pudełku, aby zachować wilgotność próbki;
H. (Krok opcjonalny) Dodaj odpowiednią ilość kropelek roztworu rozrywającego błonę do tkanki, całkowicie infiltruj tkankę, obróbka w temperaturze pokojowej przez 20 min, obróbka rozbijająca błonę kończy się tak samo po zakończeniu płukania próbki roztworem PBS, w celu usunięcia nadmiaru cieczy, po obróbce próbki w komorze mokrej, aby utrzymać próbkę mokrą.
C. Pełzanie komórek
A. Przylegające komórki hoduje się w komorach szkiełkowych Lab-Tek (szkiełko komorowe), a szkiełka delikatnie zwilża się i przemywa 2 razy PBS po leczeniu indukcji apoptozy;
B. Do każdej komory szkiełka dodaje się odpowiednią ilość utrwalacza, aby pokryć tkankę i inkubuje przez 20 minut w temperaturze pokojowej;
C. Usunąć utrwalacz i dodać PBS do przemywania 3 razy po 5 minut;
D. Każdą próbkę zanurza się w roztworze 0,2% Triton X-100 przygotowanym w PBS i inkubuje przez 5 minut w temperaturze pokojowej w celu uzyskania permeabilizacji;
mi. Przemyć próbki, zanurzając je 2-3 razy w otwartej zlewce zawierającej roztwór PBS;
F. Delikatnie usuń nadmiar płynu i za pomocą bibuły filtracyjnej ostrożnie przetrzyj ciecz wokół próbki na szkiełku. Przetworzoną próbkę umieszcza się w wilgotnym pudełku, aby zachować wilgotność próbki.
D. Rozmaz komórkowy
A. Komórki zawiesza się ponownie w PBS w stężeniu około 2 × 107 komórek/ml i 50-100 µl zawiesiny komórek aspiruje się na szkiełku zapobiegającym oderwaniu, a czyste szkiełko służy do delikatnego rozprowadzenia zawiesiny komórek;
B. Rozmazy komórkowe zanurza się w naczyniu do barwienia wypełnionym roztworem utrwalającym, komórki utrwala się i pozostawia w temperaturze 4 stopni na 25 minut;
C. Zanurz szkiełko w PBS i pozostaw w temperaturze pokojowej na 5 minut do namoczenia i wypłukania, powtórz raz;
D. Delikatnie usuń nadmiar płynu i ostrożnie osusz nadmiar płynu wokół próbki na szkiełku za pomocą bibuły filtracyjnej, za pomocą pisaka histochemicznego narysuj małe kółko wzdłuż obwodowego konturu komórki, aby ułatwić dalsze przetwarzanie przepuszczalności i operacje znakowania równowagi, i nie dopuść do próbka wyschła w trakcie doświadczenia;
mi. Każdą próbkę zanurza się w roztworze 0,2% Triton X-100 przygotowanym w PBS i inkubuje przez 5 minut w temperaturze pokojowej w celu uzyskania permeabilizacji;
F. Przemyć próbki, zanurzając je 2-3 razy w otwartej zlewce zawierającej roztwór PBS
G. Delikatnie usuń nadmiar płynu i ostrożnie przetrzyj ciecz wokół próbki na szkiełku za pomocą bibuły filtracyjnej. Utrzymuj próbkę wilgotną, umieszczając traktowaną próbkę w wilgotnym pudełku.
2. Eksperyment kontroli pozytywnej z traktowaniem DNazą I (etap opcjonalny)
Po zabiegu zwiększającym permeabilizację próbki traktuje się DNazą I (zalecany G3342) w celu przygotowania kontroli pozytywnych.
2.1. Do permeabilizowanych próbek wkrapla się 100 µl 1×DNase I Buffer (przygotowanie: pobrać 10 µl 10×DNase I Buffer, następnie dodać 90 µl wody dejonizowanej i dobrze wymieszać) i inkubować przez 5 minut w temperaturze pokojowej;
2.2. Delikatnie usunąć nadmiar płynu, dodać 100 µl roztworu roboczego zawierającego DNazę I (20 U/ml) (metoda przygotowania: pobrać 10 µL 10× buforu DNazy I, następnie dodać 2 µL DNazy I, a następnie dodać 88 µL dejonizowanego woda do wymieszania) i inkubować przez 10 minut w temperaturze pokojowej;
2.3. Delikatnie usuń nadmiar płynu i dokładnie umyj szkiełka 3-4 razy w kadzi do barwienia wypełnionej PBS.
Uwaga: Szkiełka kontroli dodatniej należy wybarwić przy użyciu oddzielnej kadzi do barwienia, w przeciwnym razie pozostała DNaza I na szkiełkach kontroli dodatniej może wprowadzić wysokie tło na szkiełka doświadczalne.
3. Znakowanie i detekcja
3.1. Równoważenie: Dodać 50 µl buforu równoważącego do każdej próbki, aby pokryć całą powierzchnię próbki i inkubować przez 10 minut w temperaturze pokojowej;
3.2. Przygotowanie roztworu do znakowania: Rozmroź mieszankę znakującą EdUTP i bufor równoważący na lodzie i wymieszaj wystarczającą ilość buforu do inkubacji TdT dla wszystkich eksperymentów zgodnie ze stosunkiem Rekombinowany enzym TdT: Mieszanka znakująca EdUTP: Bufor równoważący=1 µL:5 µL:50 µL ( 1:5:50), objętość odczynników stosowanych w poszczególnych eksperymentach można dostosować w równych proporcjach w zależności od wielkości slajdy;
3.3. System kontroli negatywnej: Przygotuj kontrolny bufor do inkubacji TdT bez rekombinowanego enzymu TdT i zastąp go ddH2O;
3.4. Etykietowanie: Usunąć jak najwięcej buforu równoważącego, następnie dodać 56 µl buforu inkubacyjnego TdT do każdej próbki tkanki i inkubować w temperaturze 37 stopni przez 1 godzinę; uważaj, aby nie wysuszyć szkiełek;
3.5. Natychmiast przemyć próbki tkanek PBS przez 4 płukania po 5 minut każde;
3.6. Reakcja Click: Usuń bufor PBS z poprzedniego etapu, dodaj kroplami 100 µl roztworu reakcji Click na próbkę tak, aby przykryła próbkę, inkubuj przez 30 min w temperaturze pokojowej z dala od światła; (system reakcji kliknięcia znajduje się w poniższej tabeli, należy dodawać każdy odczynnik po kolei, dobrze mieszając podczas dodawania, a ilość preparatu można proporcjonalnie zwiększać lub zmniejszać, zaleca się wcześniejsze jego przygotowanie)
|
Część |
Tom |
|
Bufor reakcyjny A |
925 μL |
|
Bufor reakcyjny B |
10 μL |
|
Barwnik azydkowy iF647 |
15 μL |
|
Dodatek reakcyjny (Odczynnik C) |
50 μL |
|
Całkowita objętość |
1000 μL |
3.7. Usunąć roztwór reakcji kliknięcia i natychmiast przemyć buforem PBS 2-3 razy po 5 minut;
3.8. Delikatnie wytrzyj roztwór PBS wokół próbki bibułą filtracyjną;
3.9. Barwienie jądrowe: Próbki barwi się w kadzi do barwienia, gdzie szkiełka zanurza się w ciemności do kadzi do barwienia zawierającej roztwór DAPI (świeżo przygotowany i rozcieńczony PBS) i pozostawia w temperaturze pokojowej na 8 minut (lub wykonuje się barwienie jądrowe za pomocą Hoechst 33258 );
3.10. Uszczelnianie: Po zabarwieniu próbki tkanek przemywa się trzykrotnie PBS po 5 min, następnie delikatnie usuwa się nadmiar płynu i próbki uszczelnia się kroplami uszczelniacza wygaszającego fluorescencję (zalecany G1401);
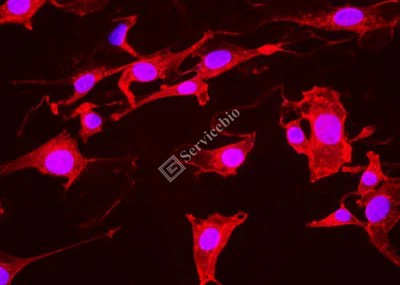
3.11. Mikroskopia: Próbki należy natychmiast przeanalizować pod mikroskopem fluorescencyjnym, szkiełka chronić przed światłem, DAPI barwi na niebiesko zarówno komórki apoptotyczne, jak i nieapoptotyczne, a jedynie w jądrach komórek apoptotycznych występuje różowa fluorescencja zlokalizowana przez domieszkę barwnika azydkowego iF647.
Tylko do użytku badawczego!
Popularne Tagi: click-it 647 zestaw do wykrywania apoptozy komórek tunelowych, Chiny click-it 647 zestaw do wykrywania apoptozy komórek tunelowych producenci, dostawcy, fabryka